Cours 1 - Sol Abiotique
Origine des sols
Tous les sols proviennent d’une __________
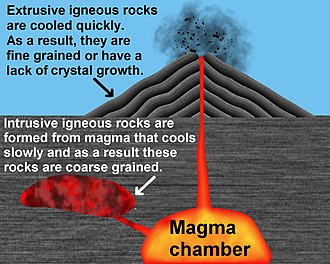
- Extrusive ou intrusive
- Temps de refroidissement et roches ultramafiques…

- Agents de cimentation
- Origine des dépôts = ?
- Falaise de Douvres (Bretagne)
Roches remodelées par la chaleur et la pression.
Variables, selon l’identité des minéraux qui ont été “remodelés” et les conditions dans lesquelles ça s’est produit…
Météorisation
Définition
Altération phyique et chimique de la roche-mère
Physique:
- Gel-dégel
- Sels
- Soleil et chaleur
- Vent
- Glaciers
- Eau
Chimique:
- Acides organiques
- CO2
- Absorption de nutriments
Exemples



Brin de terminologie
Définition
Amas de matériaux transportés par un glacier, pouvant inclure du matériel en suspension qui a été déposé par l’eau de fonte stagnante ou ralentie, et/ou des fragments rocheux fragmentés par le passage d’un glacier

Définition
Matériel déposé à l’embouchure d’un petite cours d’eau dans un plus grand, généralement de forme triangulaire. L’élargissement soudain du cours d’eau crée un fort ralentissement dans le débit, permettant la sédimentation des particules (plus grossières en premier). L’accumulation de ce matériel peut créer des zones humides pouvant devenir d’excellents sites agricoles dans certaines régions du monde.
Définition
Se dit du matériel transporté et déposé par le vent. Un loess est donc un type de sol formé à partir de particules fines, et non pas de roche-mère à proprement parler. Toutefois, l’accumulation de ce matériel transporté par le vent peut se consolider sur une très grande épaisseur (e.g., plusieurs centaines de mètres dans le plateau de Loess issu du désert de Gobi en Chine!)

Définition
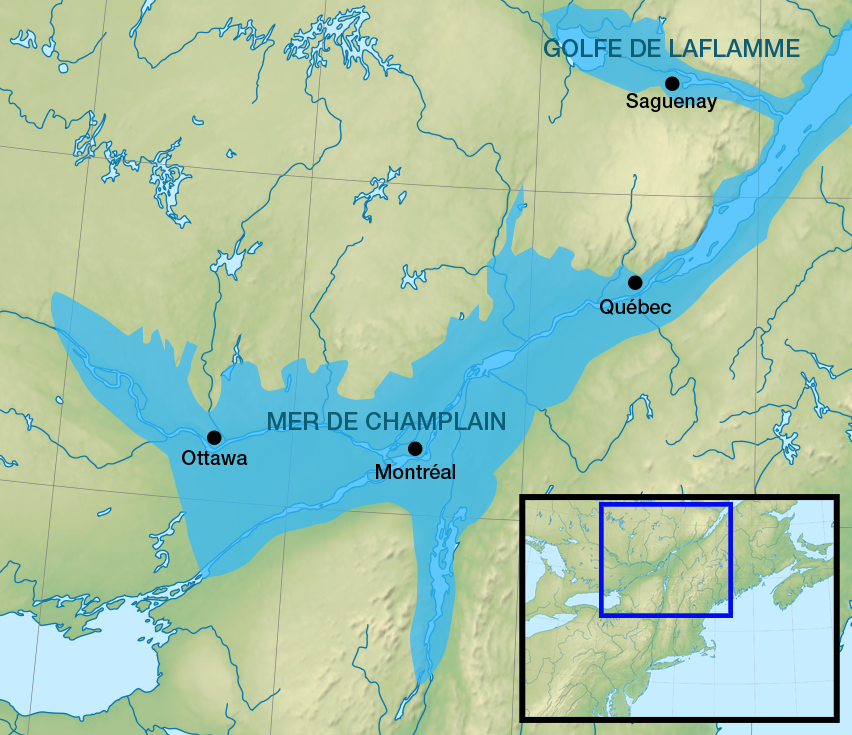
Sédiments déposés dans des lacs formés par l’eau issue des glaciers. Parfois, à plus grande échelle la fonte peut mener à la création de mers (nous sommes sur l’ancienne mer de Champlain). Les basses-terres du St-Laurent ne seraient pas aussi fertiles sans ces dépots sédimentaires datant de la dernière glaciation!
Contenu du sol

Particules minérales du sol
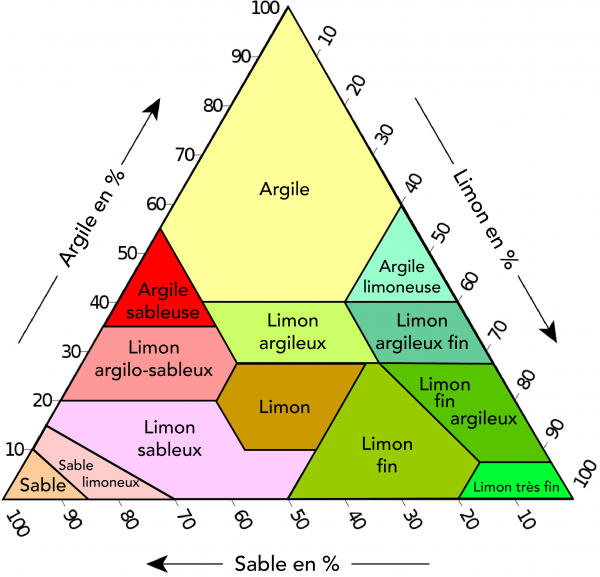

- Qu’est-ce que la loi de Stokes?
- La taille détermine le ratio surface/volume des particules… à suivre!
- 3 seuils à retenir: 2mm - 50\(\mu\)m - 2\(\mu\)m
Silicates
Définition
Silice en lien de coordination d’électrons avec 4 oxygènes formant ainsi une forme pyramidale (un tétraèdre). Le type de molécule le plus commun de la croûte terrestre.
- Le type de molécule le plus commun de la croûte terrestre
- Les oxygènes sont souvent partagés entre silicates voisins

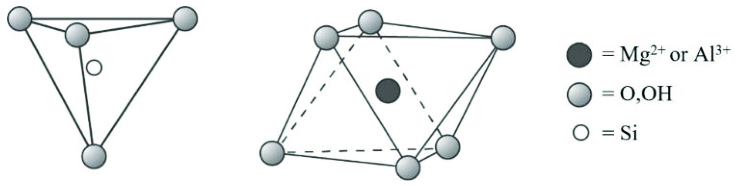
Octaèdres d’aluminium
Définition
Aluminium (peut être remplacé par autre métal divalent, e.g. Mg2+) en lien de coordination d’électrons avec 6 oxygènes formant ainsi un octaèdre (deux pyramides à bases carrées collées par leur base).
- Deuxième type de molécule le plus commun
- Composante centrale à tous les argiles
Substitution isomorphique
Définition
Remplacement d’un cation polyvalent par un autre cation, le plus souvent de valence plus faible. Par exemple, remplacement d’un Si4+ par un Al3+, ou d’un Al3+ par un Mg2+… Cela crée une charge nette permanente au tétraèdre ou octaèdre concerné.
- La source principale de charge indépendantes du pH dans le sol!
- La majorité des charges créées sont négatives
- TRÈS important pour:
- Agrégation
- Rétention de l’eau
- Capacité d’échanger/retenir des cations
Types de silicates
On va faire ça simple, en ne voyant que les deux classes principales:
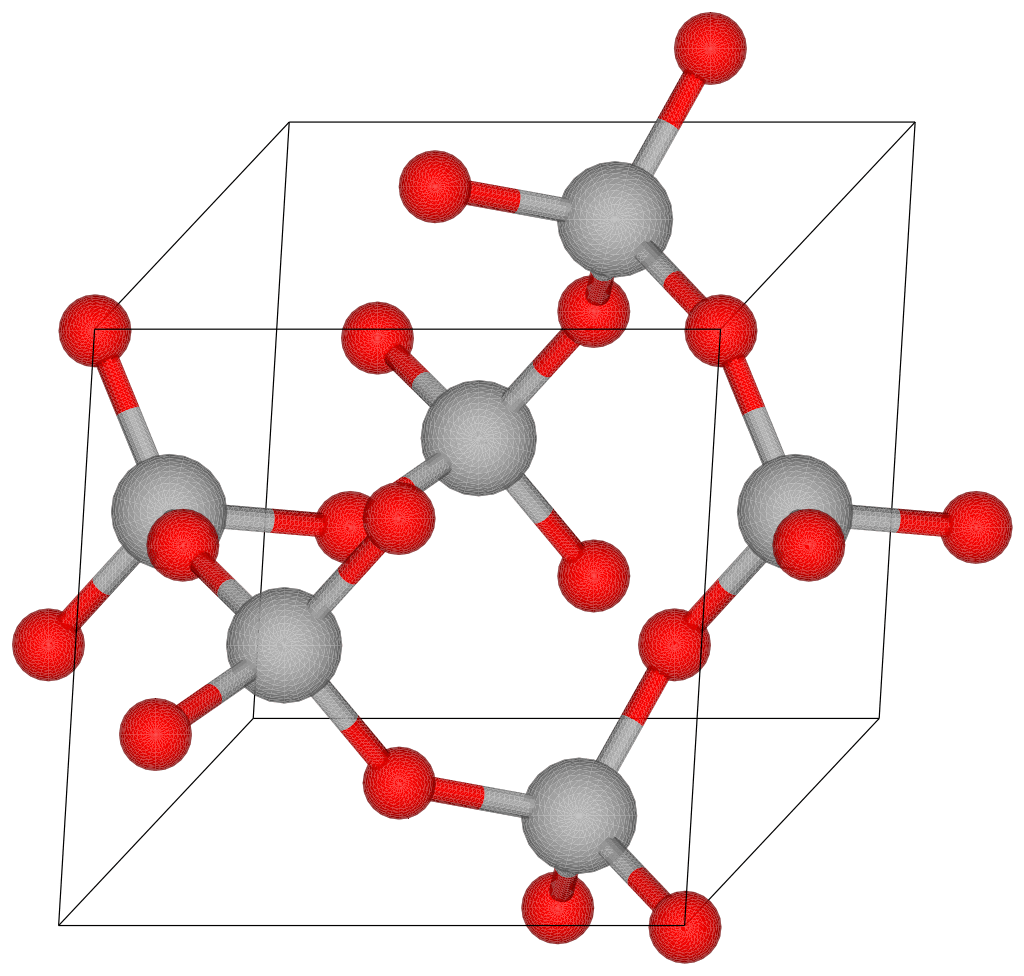
Tectosilicates
- Partage élevé et “3D” des O
- Quartz=SiO2
- Feldspaths=(MSi3AlO8)
Phyllosilicates
- Partage des O de la base des tétraèdres
- Feuillets alternant tétraèdres et octaèdres
- Conformation 2:1 ou 1:1
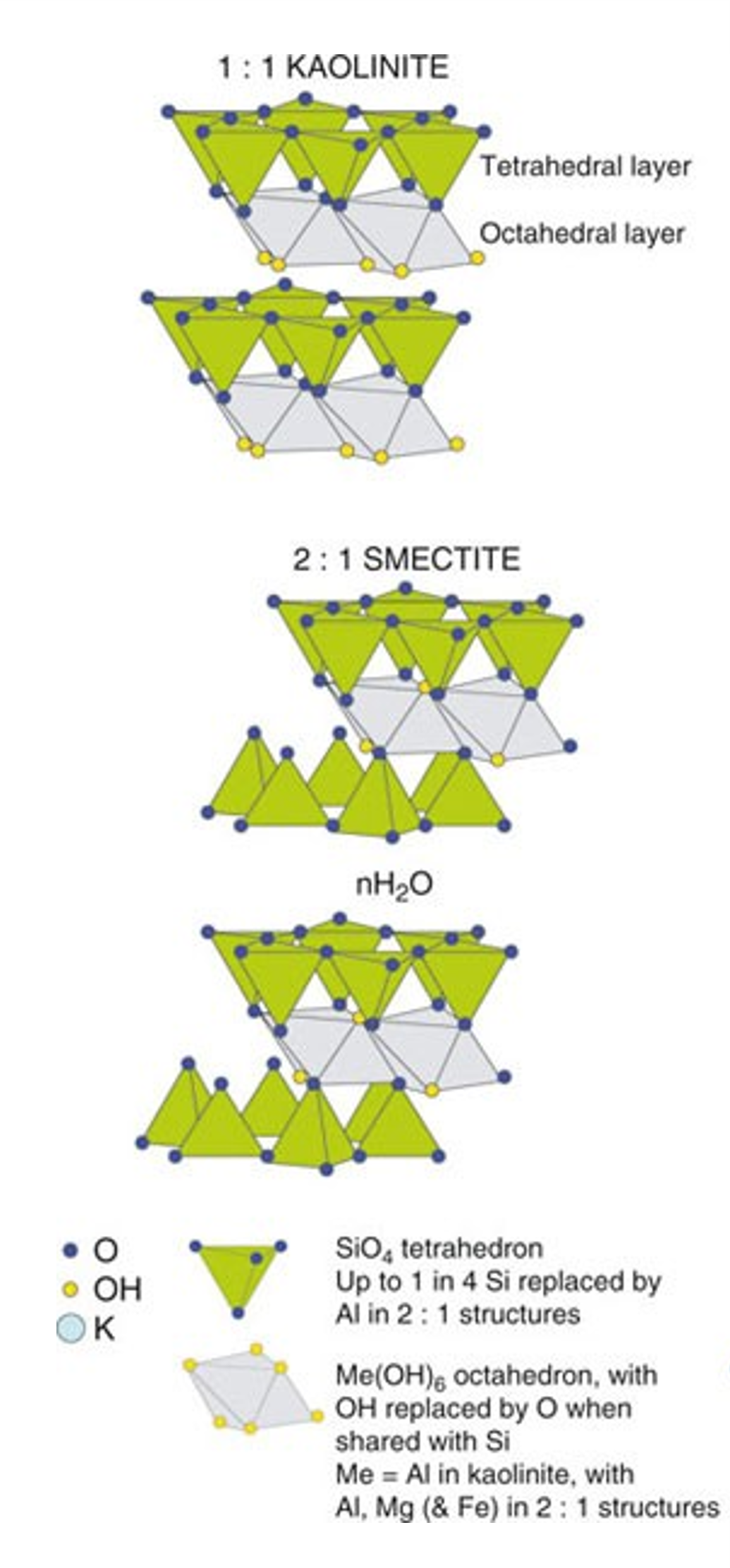
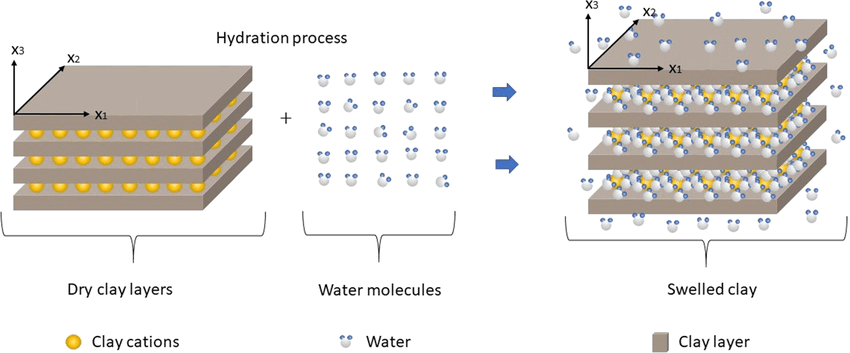
Familles de phyllosilicates
Tip
Les phyllosilicates varient selon (1) leur densité de charges (subst. isomorph.), (2) l’identité des cations qui stabilisent la charge entre les feuillets [hydratation par la bande] et (3) leur conformation générale 1:1 ou 2:1
Familles importantes:
- Micas
- Vermiculites
- Smectites


Oxydes métalliques
Définition
Molécules généralement cristallines formées par remodelage chimique de la roche-mère. Ces cristaux peuvent partager ensemble des arêtes ou des sommets (i.e., atomes de O).
Ces cristaux peuvent aussi être sites de substitution isomorphique, conférant ainsi des charges (souvent négatives, mais aussi positives parfois).
Les oxydes métalliques contribuent ainsi fortement à la capacité d’un sol à retenir et échanger des cations et des anions avec la solution liquide du sol.


Phénomènes de surface
Tip
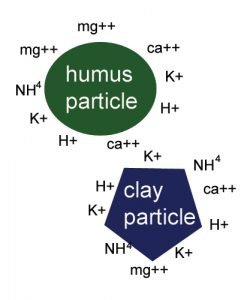
Une large majorité des phénomènes importants en pédologie se déroulent à la surface des particules minérales (silicates et oxydes métalliques en tête de liste) et de la matière organique. Entre autres parce que ces surfaces sont chargées/polaires, ce qui influence la dynamique de l’eau, des cations et des anions.
La fraction argileuse d’un sol (phyllosilicates et oxydes métalliques) et la matière organique dissoute sont présents sous forme de colloïdes
Étant en “suspension” dans l’eau du sol, ils offrent donc toutes leurs surfaces pour influencer l’agrégation, la rétention de l’eau et l’échange de nutriments!
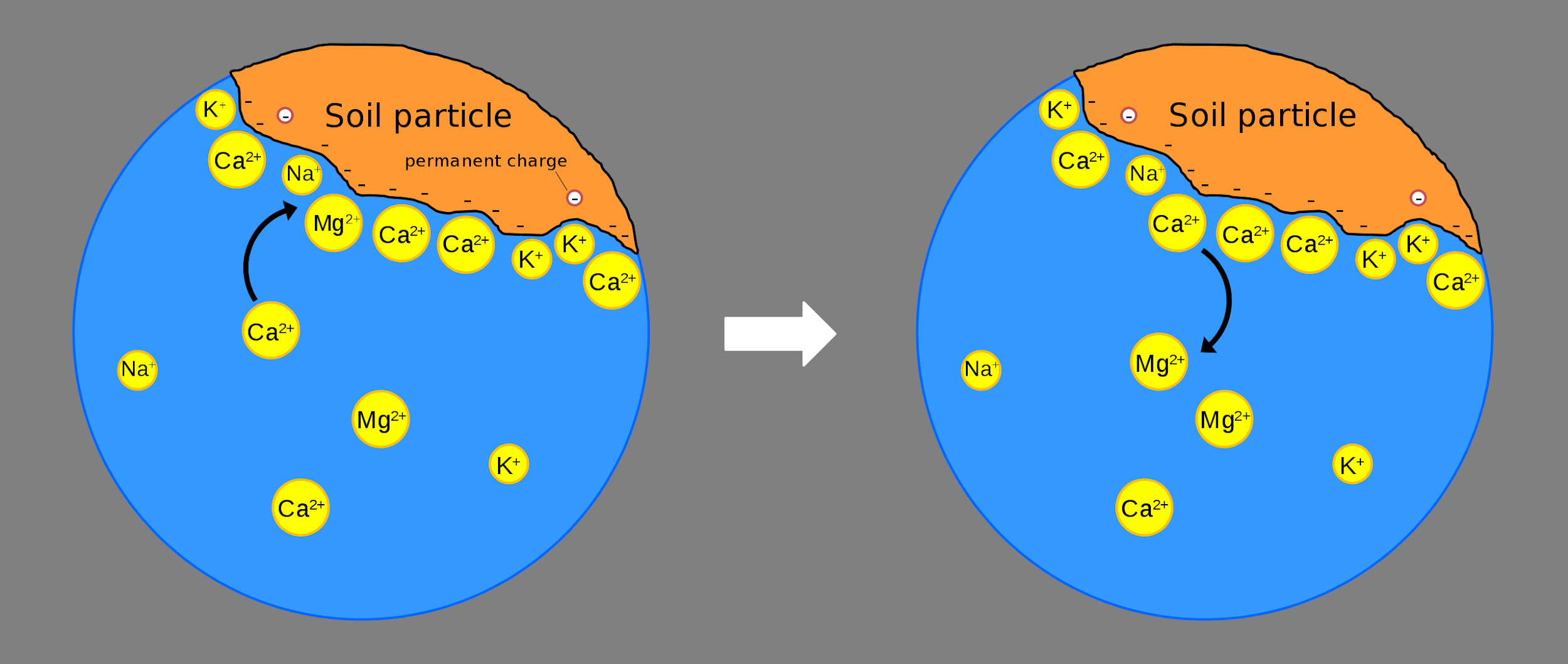
Adsorption
Se dit d’une interaction électrostatique non permanente (non covalente) entre une molécule ou un atome et un site chargé sur un colloïde du sol
Effets de masse
La propension d’un cation à se lier aux charges négatives disponibles sur les colloïdes du sol est proportionnelle à:
- Son affinité pour les sites d’échange
- Sa concentration relative dans la solution du sol
Important
Même si à chaque unité de temps, la concentration de Mg2+ adsorbée aux sites d’échange peut être relativement stable, à l’échelle de l’atome, il y a un mouvement constant. L’atome est adsorbé à un site d’échange, puis retourne à la solution de sol, puis il est adsorbé de nouveau… ainsi, si soudainement il y a une arrivée massive d’ions H+ dans la solution de sol, sa propension à être adsorbé vient de diminuer drastiquement, car soudainement il a de la compétition pour les sites d’échange!
Règle du pouce pour l’affinité aux sites d’échange:
MAIS, même avec une affinité plus faible pour les sites d’échange, un cation en assez grande concentration en déplacera un autre moins concentré!
Atmosphère du sol
Tip
L’air dans le sol voyage par diffusion, un mouvement généralement plus lent que la convection.
- Loi de Fick
- Connectivité entre les pores (aération)
- Importance de la teneur en eau
Porosité du sol:
Échelle de gris = densité de matériel solide (tomographie rayons X)
Échelle couleur = estimation de porosité modélisée (\(\phi\))
Oxydo-réduction du sol
Définition
Une réaction qui permet le transfert d’électrons d’un donneur à un accepteur.
- L’accepteur suprême: O2
- Les processus les plus influencés:
- Respiration cellulaire
- Modifications chimiques des composantes du sol
- E.g. \(\ce{Fe^2+<=>Fe^3+}\)

L’eau du sol
L’eau est le solvant par excellence du sol, le véhicule permettant les flux de nutriments, et ce qui ultimement permet aux plantes de transpirer.
Les nutriments voyagent soit par diffusion (lente) our par flux de masse, selon leur affinité pour les sites d’échange. Les nitrates
(\(\ce{NO3-}\)) voyagent par flux de masse, alors que les phosphates
(\(\ce{PO4^3-}\)) voyagent faiblement, par diffusion…
Forces en jeu
Les forces en jeu déterminant les mouvements de l’eau sont la gravité, les forces adhésives et les forces cohésives
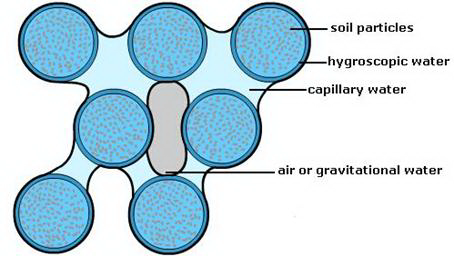
TERMES IMPORTANTS
- Capacité au champ
- Eau gravitationnelle
- Eau capillaire
- Micropores
- Macropores
Tension superficielle
L’eau capillaire est retenue dans le sol due à la grande tension superficielle caractéristique aux films d’eau. Cette molécule polaire faisant des ponts H avec elle-même tend à générer des films très difficiles à briser!
Matière organique
Pédogenèse et matière organique
L’augmentation des stocks de matière organique dans le développement d’un jeune sol est un fait saillant central. La roche-mère est généralement largement dépourvue de matière organique et d’azote.
D’OÙ PROVIENT LA MATIÈRE ORGANIQUE?
- Biomasse morte (nécromasse), provenant de différents organismes vivants (plantes et microorganismes en tête)
- Composés exsudés par les organismes vivants (e.g., sucres, acides organiques, acides aminés, etc.)
La matière organique se présente souvent sous forme de colloïde dans le sol, et porte un grand nombre de charges, surtout négatives. Elle contribue donc à la capacité d’échange cationique et anionique du sol.
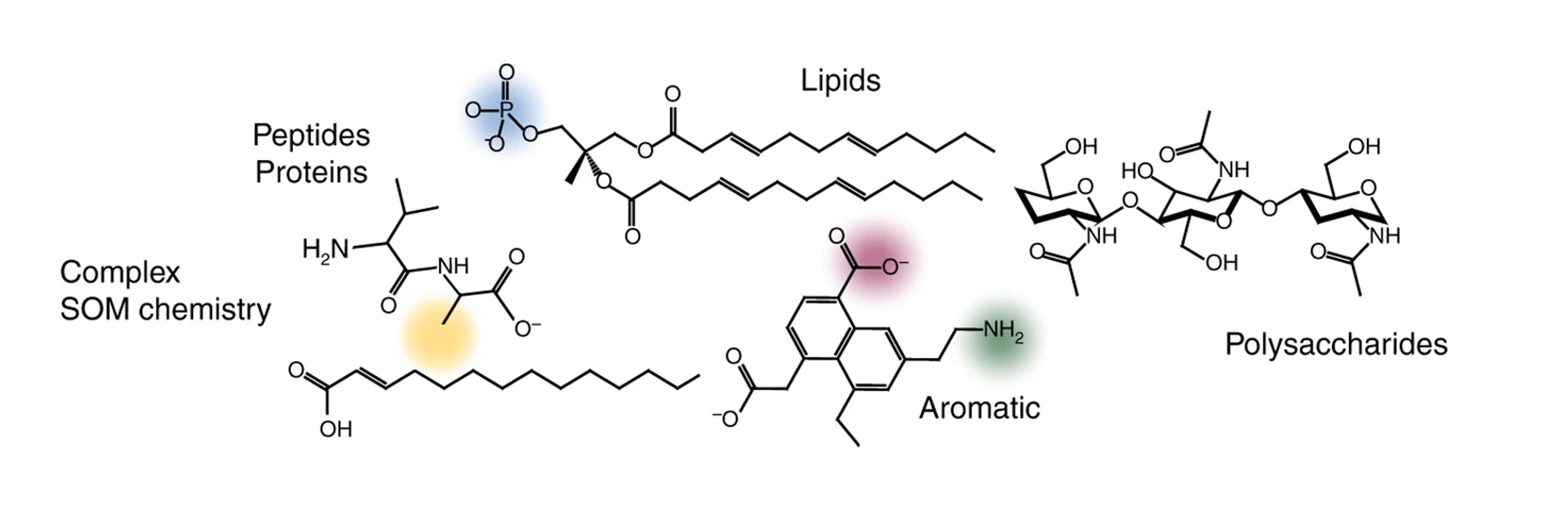
Rôles de la matière organique du sol
- Échanges cationiques et anioniques
- Agrégation
- Carburant
- Réserve de nutriments
- Rétention d’eau
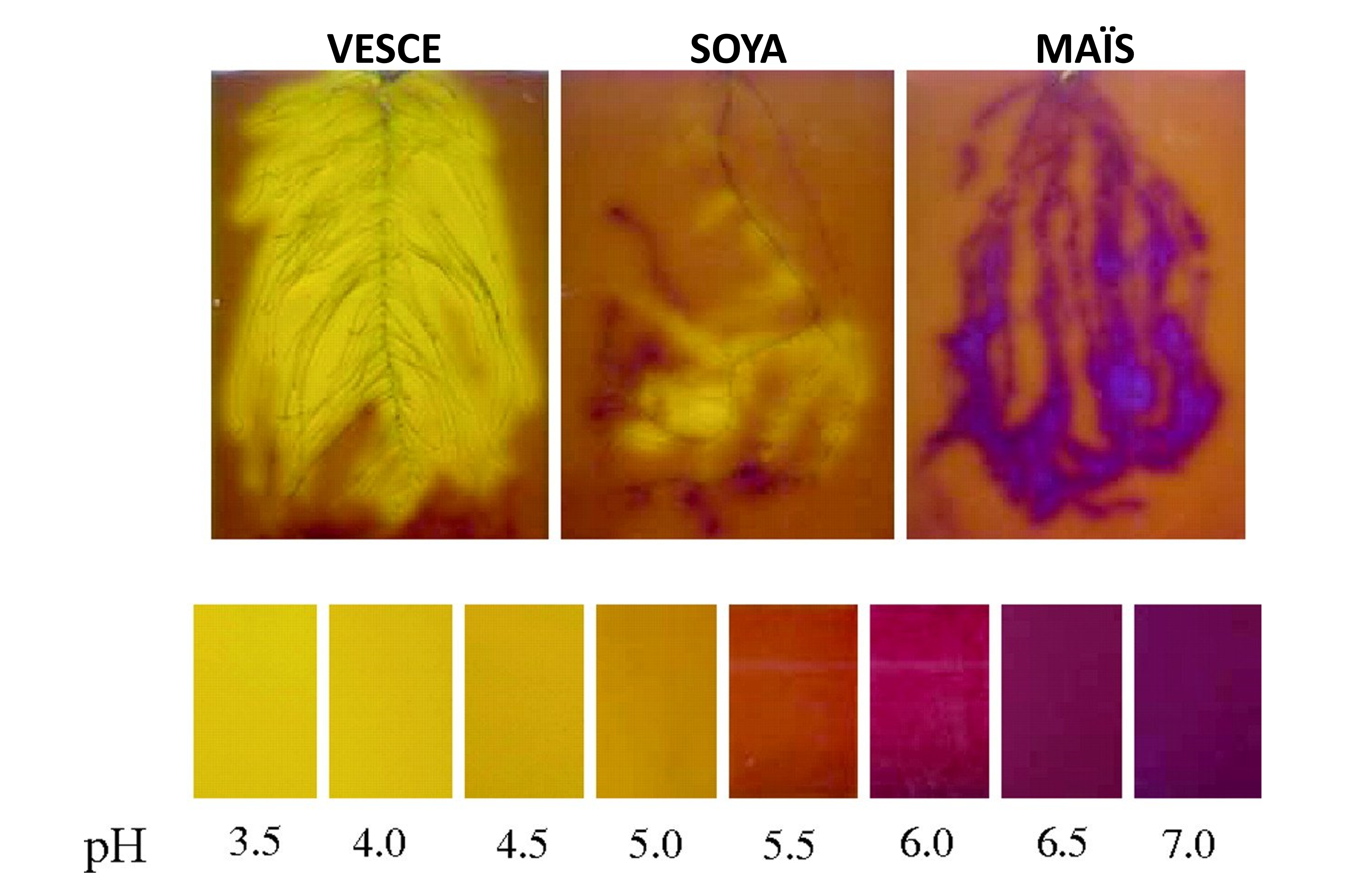
pH du sol
\[pH = -log[\ce{H^+}]\]
Plus il y a de H+ dans le sol, et:
- Moins il y a d’agrégation (compétition avec les cations divalents)
- Moins certains nutriments sont disponibles (N-P-K-S-Ca-Mg)
- Plus d’autres nutriments sont disponibles (Fe-Mn-B-Cu-Zn)
- Plus le risque de toxicité par l’aluminium est élevé
- Moins il y a de charges négatives disponibles pour les autres cations (effets de masse)
Toutefois, notez qu’il y a certaines charges qui sont pH indépendantes : les charges issues de la substitution isomorphiques sur les particules minérales.
pH dans le monde
Facteurs influençant le pH mondial
Deux processus majeurs influencent le pH: le type de végétation et les précipitations effectives
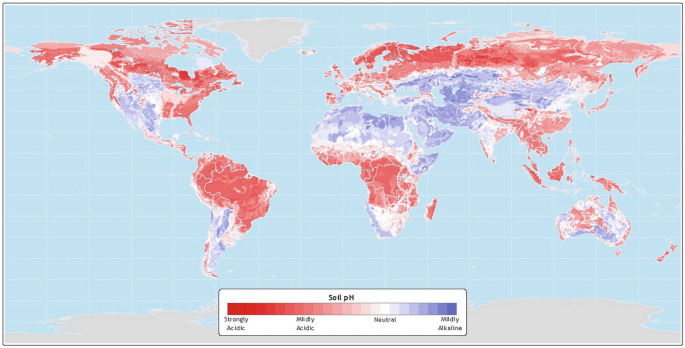
Une température chaude et humide favorisent:
- La météorisation (libération des cations alcalins vers la solution du sol)
- Le lessivage de ces cations lorsque beaucoup d’eau gravitationnelle passe au travers du sol
Cations alcalins
Tous les cations qui ne libèrent PAS de H+ en réagissant avec l’eau. Il s’agit de Ca2+, Mg2+, Na+, et K+. Par opposition, les cations acides sont le Fe3+ et le Al3+, qui ont un ratio charge/rayon atomique assez élevé pour dissocier l’eau et relâcher des H+ en solution.
On voit clairement que les sols les plus alcalins du monde sont développés là où l’écosystème est dominé par de la prairie/savanne, et non pas par de la forêt.
Les sols les plus acides sont:
- Les podzols de la forêt boréale
- Les oxisols et ultisols des forêts tropicales humides
